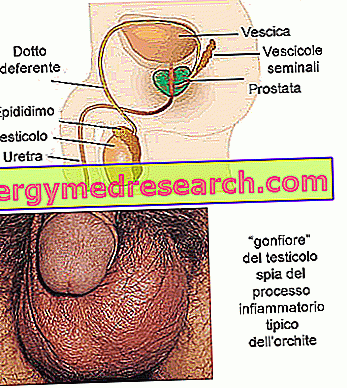
Антифунгали - или антифунгали - су лекови који се користе за лечење инфекција узрокованих гљивицама, укључујући квасце и плијесни. Ове инфекције се називају микозе .
увод

Међутим, овај аргумент се не односи на појединце с имуном компромитацијом. У ствари, ширење АИДС-а и употреба моћних имуносупресивних лијекова у превенцији одбијања трансплантација и кемотерапије рака, повећали су учесталост потенцијално смртоносних гљивичних инфекција. Због тога се јавила потреба за развојем све ефикаснијих и безбеднијих антифунгалних лекова.
Тешкоће у развоју антифунгалних лекова леже у високој селективности коју морају да имају. У ствари, разлике између ћелија гљивица и ћелија сисара су веома мале, јер су обе еукариотске ћелије.
Међутим, иако су минималне, постоје неке разлике између ова два типа ћелија:
- Присуство ћелијског зида у гљивичним ћелијама, али не и код сисара;
- Састав ћелијских мембрана. Посебно, ћелијске мембране гљивица се разликују од оних код сисара за стероле присутне у њима. Стероли су неопходне компоненте ћелијске мембране; ергостерол је присутан у ћелијама гљивица, док је холестерол присутан у ћелијама сисара.
Стога је јасно зашто станични зид и ергостероли представљају два главна циља антифунгалне терапије.
Класе антифунгалних лекова
Укратко, циљеви за антифунгалну терапију која је селективна само за гљивичне ћелије су у суштини два: ћелијски зид гљивица и ергостерол садржан у ћелијској мембрани.
Због тога, већина антифунгалних лекова делује тако што уништава или омета синтезу ове две фундаменталне компоненте за гљивичне ћелије.
Класе антигљивичних лекова које се тренутно налазе на тржишту биће укратко описане у наставку.
Антифунгали који мењају ћелијску мембрану
Са хемијске тачке гледишта, ови антифунгални лекови су полиени, тј. Они су алифатски угљоводоници који садрже бројне двоструке везе угљеник-угљеник у оквиру њихове хемијске структуре.
Ови полиени имају висок афинитет за ћелијске мембране које садрже стерол. Конкретније, полиени имају велики афинитет за мембране које садрже ергостерол (као што су оне гљивичне).
Ови лекови су способни да стану унутар ћелијске мембране и повећају њихову пропустљивост. Ово повећање доводи до тога да ћелије губе састојке који су неопходни за њих (као што су јони и мали органски молекули) и - сходно томе - умиру.
Нистатин, амфотерицин Б и натамицин припадају овој класи лекова.
Инхибитори биосинтезе Ергостерол
Ови лекови делују тако што инхибирају један од кључних ензима синтезе ергостерола, 14а-деметилаза.
Са инхибицијом овог ензима долази до акумулације прекурсора ергостерола; ова акумулација ствара промене у пропустљивости ћелијске мембране и изазива промене у функционисању мембранских протеина, осуђујући тако ћелије гљивица до сигурне смрти.
Лијекови који припадају овој класи су бројни; то укључује кетоконазол, итраконазол, терконазол, флуконазол, вориконазол и посаконазол .
Инхибитори сквален епоксидазе
Сквален епоксидаза је ензим који је укључен у процес синтезе ергостерола.
Нарочито, овај ензим претвара сквален (прекурсор ергостерола) у сквален епоксид (други прекурсор ергостерола) који се - након других ензиматских реакција - затим трансформише у ергостерол.
Инхибиција узрока сквален епоксидазе:
- Смањење укупног садржаја ергостерола у ћелијској мембрани гљивица, то доводи до промена у пропустљивости саме мембране и неисправности мембранских протеина укључених у транспорт хранљивих материја и у регулацији пХ ћелија;
- Акумулација сквалена у ћелији гљивица која - када достигне превелике количине - постаје токсична за саму ћелију.
Све то доводи до смрти ћелије гљивица.
Ова класа антифунгала укључује нафтифину, тербинафин, толнафтат и аморолфин .
Инхибитори биосинтезе гљивичне ћелијске стијенке
Ова антифунгална средства инхибирају један од ензима укључених у синтезу гљивичне ћелијске стијенке, β-1, 3-глукан синтазе. Овај ензим је одговоран за синтезу β-глукана, који је основни елемент ћелијског зида. Смањење количине β-глукана у зиду узрокује да ослаби да изазове лизију гљивичне ћелије.
Каспофунгин, анидулафунгин и микафунгин спадају у ову класу лекова.
Антифунгални лекови који делују са другим механизмима
Постоје и антифунгални лекови који не ометају синтезу ћелијског зида или мембранске стероле, али делују са различитим механизмима.
Међу овим лековима налазимо:
- Флуцитосина : то је снажан антифунгал који нема цитотоксичну активност (токсично за ћелију) пер се. Флуцитосине је заправо пролек који се интернализује у ћелијама гљивица и овде се метаболише у 5-флуороурацил (цитотоксични агенс) који се - након даљег метаболизма - претвара у 5-флуородеоксиуридин, метаболит способан да интерферира са синтеза протеина. 5-флуороурацил се такође користи као такав у анти-туморској хемотерапији.
- Грисеофулвин : овај лек је антифунгални антибиотик изведен из одређеног соја рода Пенициллиум . Грисеофулвин се углавном користи у лечењу површинских микоза. Једном примењен орално, грисеофулвин може да се инкорпорира у кератин и спречи раст гљивица. Надаље, чини се да овај лијек може ометати синтезу микотске ДНА.
- Циклопирокс : овај лек се углавном користи у лечењу површинских гљивичних инфекција. Циклопирокс има веома посебан механизам деловања, то јест, он је у стању да келира (то јест да се веже преко одређених типова веза дефинисаних као "координативне" или "координационе") поливалентне катионе - као што је, на пример, Фе3 + - и тако изазива инхибицију ензима зависних од метала који се налазе у ћелији гљивица.
- Ундецилениц ацид : овај антифунгал се углавном користи у инфекцијама које изазивају дерматофити (гљивице одговорне за инфекције коже, ноктију и косе). Међутим, ундециленска киселина није у стању да убије гљивичну ћелију, али има фунгистатско дејство (тј. Инхибира гљивичну пролиферацију) и врши своју интеракцију на не-специфичан начин са компонентама ћелијске мембране.